Que Es Una Reaccion Quimica De Oxido Reduccion
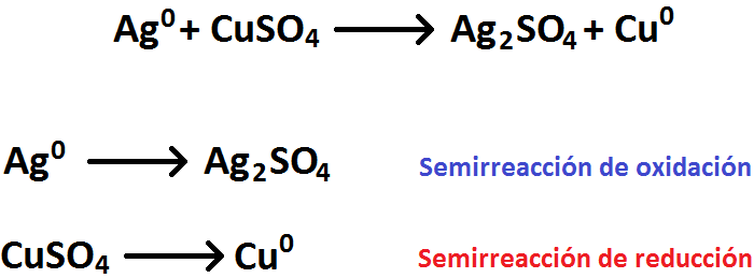
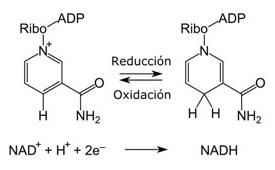
La reaccion de oxidacion reduccion que se produce durante un proceso electroquimico se compone de dos medias reacciones uno que representa el proceso de oxidacion y un proceso de reduccion.

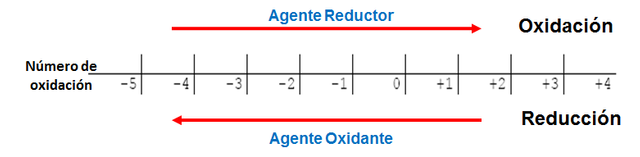
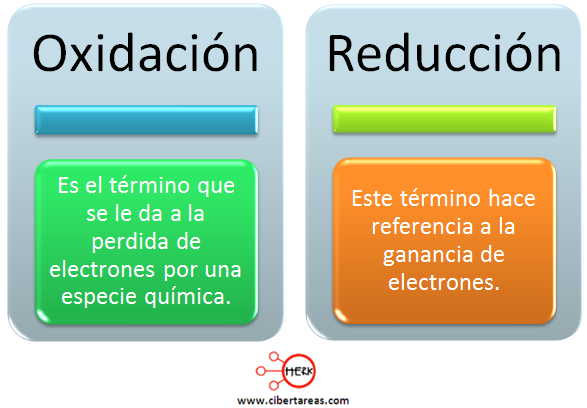
Que es una reaccion quimica de oxido reduccion. Antoine laurent lavoisier dejo un legado importante en la quimica que nos ayuda actualmente a comprender el comportamiento de las reacciones sabemos que la masa permanece constante durante la reaccion pero para comprender el mecanismo debemos de entender que detras de cortinas existen otros fenomenos que son indispensables para redondear el fenomeno como tal. Estas reacciones tambien se conocen como redox. La sustancia que pierde electrones aumenta su numero de oxidacion. Las reacciones que implican la transferencia de electrones entre las sustancias que participan se las conoce como reacciones de oxido reduccion o bien simplemente como reacciones redox.
La sustancia que gana electrones disminuye su numero de oxidacion. El agente oxidante es aquel elemento quimico que tiende a captar esos electrones quedando con un estado de. Normalmente en una reaccion de combustion se combina el oxigeno con un hidrocarburo para formar dioxido de carbono y agua. Este proceso se llama reduccion.
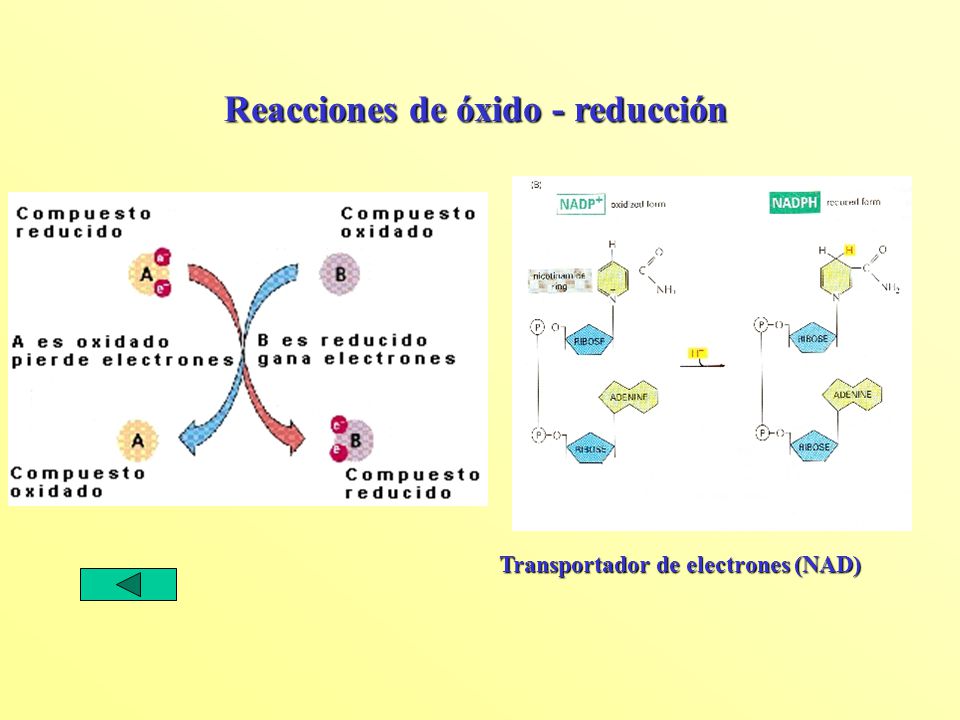
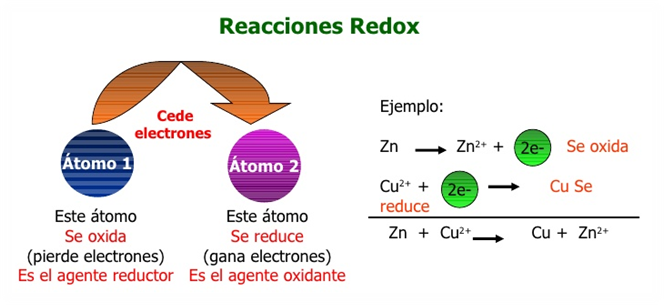
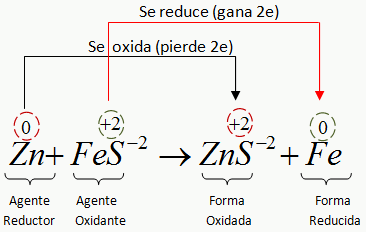
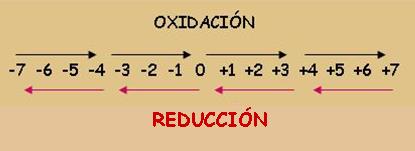
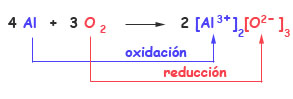
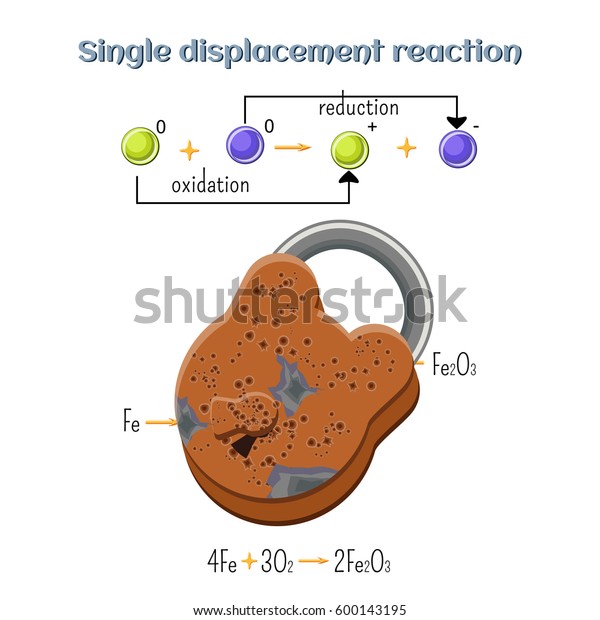
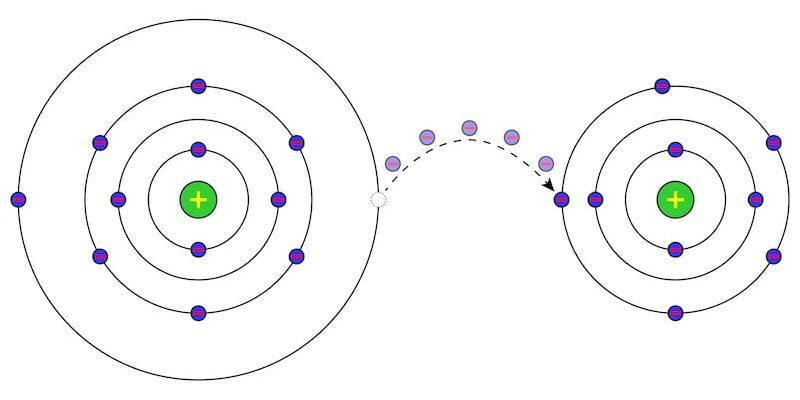
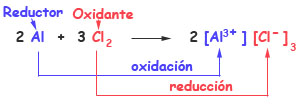
En las reacciones de oxido reduccion ocurre transferencia de electrones donde un atomo pierde electrones oxidacion y otro gana electrones reduccion ambos procesos ocurren en forma simultanea pues si un atomo pierde electrones necesariamente otro debe ganarlos. La reaccion redox general es equilibrada cuando el numero de electrones perdidos por el reductor es igual al numero de electrones ganados por el oxidante. Se denomina reaccion de reduccion oxidacion oxido reduccion o simplemente como reaccion redox a toda reaccion quimica en la que uno o mas electrones se transfieren entre los reactivos provocando un cambio en sus estados de oxidacion. Las reacciones de oxido reduccion o tambien llamadas reacciones redox son las reacciones quimicas donde uno o mas electrones se transfieren entre los reactivos provocando un cambio en el estado de oxidacion de cada uno de ellos.
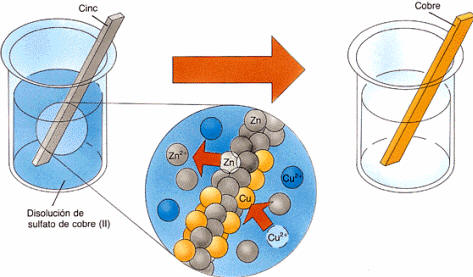
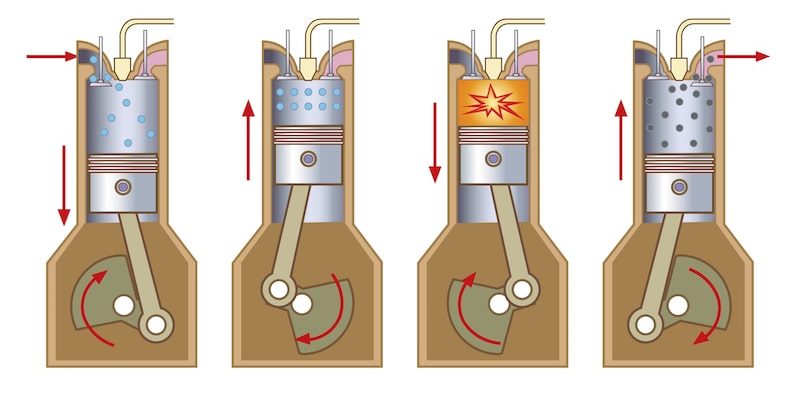
Una reaccion de oxido reduccion se caracteriza porque hay una transferencia de electrones en donde una sustancia gana electrones y otra sustancia pierde electrones. Un ejemplo es la combustion del butano. Se definen particularmente 2 tipos de reacciones en funcion a esta transferencia electronica. 2 c 4 h 10 13 o 2 8 co 2 10 h 2 o otro ejemplo es la respiracion de los seres vivos en la que se produce co 2 y h 2 o a partir del oxigeno del aire y la glucosa.
Una corriente electrica se produce a partir del flujo de electrones. Para que exista una reaccion de reduccion oxidacion en el sistema debe haber un elemento que ceda electrones y otro que los acepte.























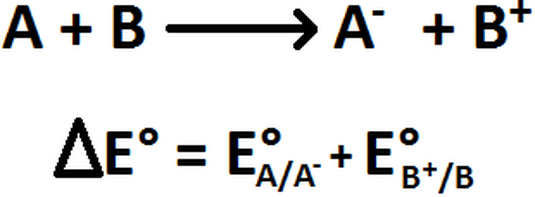

































/Redox_reaction-589cb4c83df78c47581a25a6.jpg)